Sensibilizzazione centrale: una panoramica generale
La sensibilizzazione centrale è un normale meccanismo adattativo che permette la protezione di una zona lesionata.
Quando parliamo di sensibilizzazione centrale, di solito pensiamo a un fenomeno con un inquadramento patologico. Tuttavia, spesso ci dimentichiamo che la sensibilizzazione centrale è un normale meccanismo adattativo che permette la protezione di una zona lesionata. Quando ci facciamo male, la prima risposta dell’organismo è generalmente una risposta stereotipata e vivace, che ha il compito di mettere in allarme il sistema. In condizioni normali questo processo è assolutamente reversibile: al cessare dello stimolo periferico, sia il nocicettore che il neurone centrale tornano alla normalità.
Può succedere però, che al fermarsi dell’infiammazione periferica, il neurone centrale non ritorni allo stato iniziale. In questo caso, allora, la sensibilizzazione centrale si configura come un fenomeno parafisiologico, sostenuto da cambiamenti neuroplastici.
Cos’è la sensibilizzazione centrale?
La sensibilizzazione centrale si configura come un aumento della reattività dei neuroni nocicettivi del sistema nervoso centrale al loro input afferente normale o sotto soglia (1). Questo aumento di reattività dei neuroni di secondo ordine è una risposta adattativa che ha il compito di proteggerci da un danno in atto o potenziale. Tuttavia, se sono presenti stimoli nocicettivi intensi, duraturi e ripetuti, il neurone centrale può rimanere sensibilizzato anche dopo la cessazione dello stimolo che l’ha attivato. La sensibilizzazione delle fibre è responsabile di una serie di manifestazioni quali iperalgesia secondaria (aumentata risposta a stimoli dolorosi al di fuori della zona di lesione o infiammazione), allodinia (aumentata risposta a stimoli normalmente non dolorosi anche al di fuori della zona di lesione o infiammazione), allargamento del campo recettoriale del neurone (2).
Tutto questo si traduce in un quadro clinico abbastanza tipico, caratterizzato da: dolore spesso discontinuo, non prevedibile e non coerente tra stimolo e risposta; dolore con distribuzione anatomica variabile; irritabilità, iperalgesia e after-sensation; disestesie varie; ipersensibilità a luce, suoni, tatto; dolore che non risponde a FANS; affidabilità degli esami clinici molto bassa (3)(4).
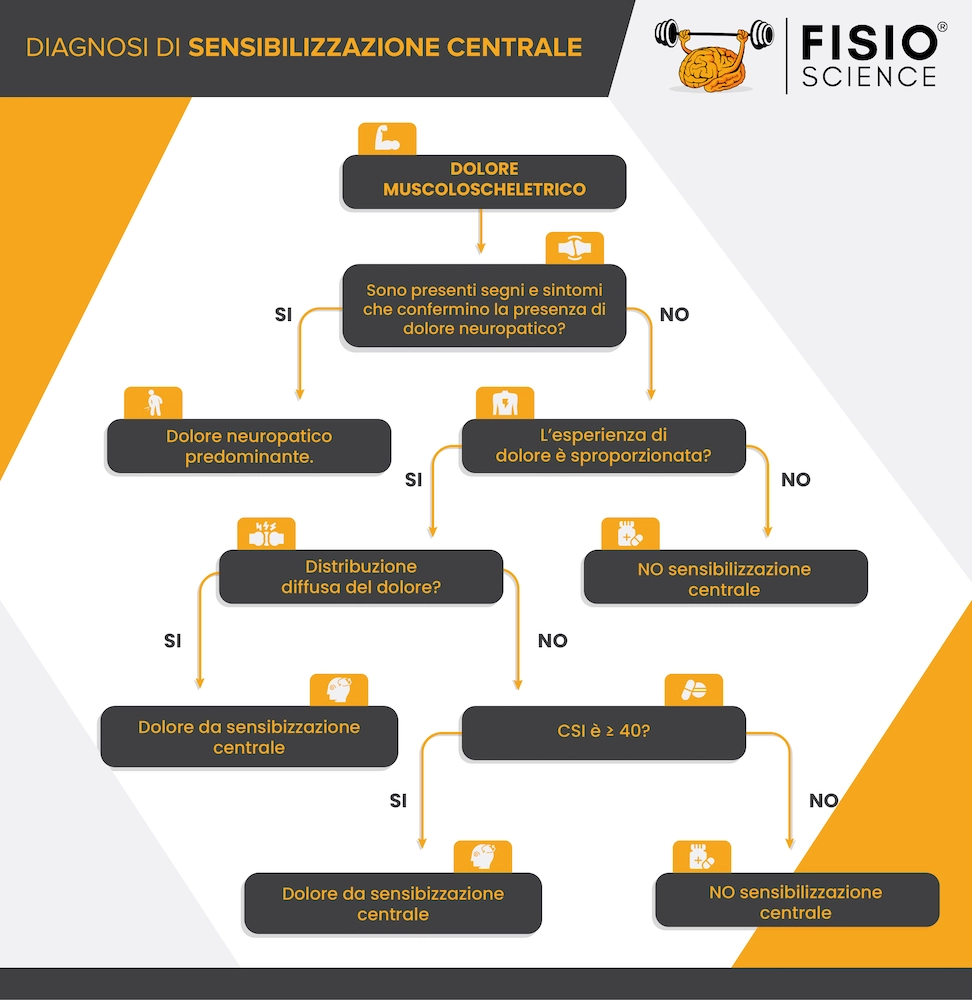
Per capire se siamo di fronte a un quadro di sensibilizzazione centrale prima di tutto dobbiamo escludere un ipotetico dolore neuropatico. Una volta esclusa questa opzione, possiamo affidarci a un algoritmo basato su tre criteri fondamentali (5): il primo criterio ha a che fare con la non proporzionalità tra dolore e natura ed entità della lesione ed è un criterio obbligatorio per la classificazione del dolore da sensibilizzazione centrale.
Il secondo criterio riguarda la distribuzione del dolore non coerente. In particolare possiamo trovare dolore diffuso e poco localizzato, distribuzione non segmentale del dolore, dolore che cambia spesso localizzazione anatomica, dolore bilaterale o mirror pain e iperalgesia o allodinia al di fuori delle zone di nocicezione primaria. Se entrambi questi criteri sono presenti, si può confermare un quadro di sensibilizzazione centrale.
Se la situazione risulta poco chiara, si indaga il terzo criterio, avvalendosi della Parte A del Central Sensitization Inventory (CSI) (6). Qui viene indagata la presenza di ipersensibilità ad altri stimoli come odori, luce, suoni, tatto, sensazione di caldo e freddo. Un punteggio al CSI ≥ 40 è fortemente indicativo della presenza di sensibilizzazione centrale. In aggiunta a questi criteri, la sensibilizzazione centrale è fortemente legata ad altri segni e sintomi come intorpidimento, debolezza muscolare, deficit dell’attenzione, disturbi del sonno. In anamnesi i pazienti riportano spesso storia di fallimenti terapeutici, intollerabilità a determinati tipi di trattamento o mancato beneficio degli stessi. Infine vi è una forte associazione con fattori psicosociali disadattativi, quali emozioni negative, scarso livello di self-efficacy, credenze errate, comportamenti di evitamento, paura del movimento, catastrofizzazione, stress. L’uso del Central Sensitization Inventory ci aiuta a capire quanto i fattori emozionali intervengano nel rinforzare i meccanismi di sensibilizzazione centrale.
Il vantaggio di possedere questi criteri di classificazione risiede nella capacità di poter attuare delle strategie terapeutiche adeguate al tipo di dolore presentato dal paziente. Gli obiettivi di trattamento di un dolore da sensibilizzazione centrale saranno ben diversi da quelli di un dolore nocicettivo! Non è semplice far capire al paziente che il problema non risiede più a livello tissutale, ma riguarda il modo in cui l’esperienza dolore viene processata (7). A livello fenotipico, la sindrome da sensibilizzazione centrale può assumere diverse forme, che includono fibromialgia, sindrome dell’intestino irritabile, cefalea tensiva, disturbi temporomandibolari, sindrome delle gambe senza riposo, sindrome da stanchezza cronica, cistite interstiziale, artrite reumatoide, osteoartrosi, complex regional pain syndrome (CRPS) (8). La suscettibilità a sviluppare ipersensibilità del sistema nervoso centrale è in parte legata anche a una componente genetica ereditaria (9)(10).
I meccanismi neurofisiologici alla base della sensibilizzazione centrale
Alla base della sensibilizzazione centrale ci sono dei cambiamenti neurofisiologici sostenuti da modificazioni neuroplastiche dell’eccitabilità neuronale (11). Quando un nervo riceve informazioni inizia ad adattarsi: si riduce la sua soglia di attivazione e aumenta il numero dei recettori per migliorare la capacità del nervo di ricevere informazioni. Dal punto di vista molecolare, aumenta il numero dei canali del sodio a livello sinaptico e con essi la facilità con cui sono disposti ad aprirsi. Quando il nervo diventa più responsivo, succede che un singolo stimolo possa attivare più recettori con soglie di attivazione più basse. Questi meccanismi sono sostenuti dal fenomeno wind-up, dove stimoli e costanti e ripetuti nel tempo aumentano la responsività delle fibre C (12), e dal Long Term Potentiation (LTP), dove l’aumentata responsività rimane anche dopo la cessazione dello stimolo (13). Il risultato è una iperresponsività del neurone periferico, come risposta adattativa avente l’intento di proteggerci da un danno o una lesione. Tutto ciò è assolutamente fisiologico. A parità di stimoli in entrata, se il neurone periferico è sensibilizzato, manderà un messaggio aumentato per il neurone spinale. Queste fibre, Higth threshold (HT), Low-threshold (LH), Wide-dynamic-range (WDR), ricevono più informazioni e iniziano anche loro ad adattarsi. Il fenomeno della sensibilizzazione inizia a ricevere connotati patologici quando il neurone di II ordine rimane sensibilizzato al cessare dello stimolo proveniente dal neurone di I ordine. I meccanismi plastici in questo caso non sono più attività-dipendenti ma diventano attività-indipendenti, come se il neurone spinale si automantenesse (11). In questo caso, il cambiamento funzionale è ancora reversibile.
Lo stato di sensibilizzazione viene mantenuto e potenziato dal rilascio di citochine pro-infiammatorie da parte delle cellule gliali che, quando iperattivate, provocano una vera e propria neuro-infiammazione (14). Oltre alle citochine, aumenta anche il rilascio di un altro neurotrasmettitore, il glutammato. Il glutammato, prodotto in situazioni di stress mantenuto, aumenta l’effetto eccitatorio sul sistema nervoso centrale, con effetto tossico sui neuroni discendenti inibitori (15). Un eccesso di glutammato infatti ne causa la morte e come conseguenza si ha un allargamento del campo recettoriale del neurone spinale, con possibile dolore riferito (16). A questo punto, iniziano a instaurarsi dei veri e propri cambiamenti strutturali a livello dell’ippocampo e della corteccia pre-frontale. Alla diminuzione di materia grigia di queste zone si associa un aumento controlaterale della materia grigia dell’amigdala, responsabile della coloritura emotiva del dolore (17). Emozioni negative, ansia, paura, catastrofizzazione e anticipazione delle conseguenze non faranno altro che mantenere attivi tutti questi cambiamenti corticali disfunzionali (18). Si ha così una vera e propria alterazione della modulazione discendente inibitoria.
Sensibilizzazione centrale e periferica
Sappiamo quindi che il neurone di secondo ordine può rimanere sensibilizzato quando riceve stimoli intensi, duraturi e ripetuti. Ma cosa succede al neurone di primo ordine?
L’insieme dei cambiamenti che avvengono nei neuroni di primo ordine prende il nome di sensibilizzazione periferica. In seguito a un danno o una lesione, si attiva un processo infiammatorio con rilascio di mediatori chimici come serotonina, bradichinine, prostaglandine e citochine. Questi mediatori attivano e sensibilizzano le fibre afferenti, creando un aumento di attività e una riduzione della soglia di attivazione dei nocicettori. Si innesca così il fenomeno dell’iperalgesia primaria, ossia un aumento della risposta agli stimoli nocicettivi, necessaria per la protezione della lesione durante il processo di guarigione (19). La sensibilizzazione periferica, essendo dovuta allo stimolo di sostanze algogene, è una sensibilizzazione transitoria e protettiva. I due tipi di sensibilizzazione differiscono tra loro per i meccanismi neurofisiologici di base e per il tipo di manifestazione clinica (20).
Sensibilizzazione centrale e dolore nociplastico: qual è la differenza?
Per definizione della IASP, il dolore nociplastico è dato da un’alterazione della nocicezione, in mancanza di un chiaro segno di danno tissutale reale o potenziale che causa l’attivazione dei nocicettori periferici o in assenza di una lesione al sistema somatosensoriale (21). Esso è dovuto alla plasticità del nocicettore e del nocineurone che sono diventati ipersensibili. Questa nuova definizione giustifica la presenza del dolore che non è specificatamente nocicettivo o neuropatico, ma che può essere considerato una via di mezzo tra i due (22). Tuttavia, si riferisce solo a quei pazienti in cui può essere dimostrata un’alterazione della nocicezione e non può essere applicato ai pazienti che presentano dolore senza ipersensibilità (23). In aggiunta, non sono ancora stati definiti dalla IASP i criteri esatti per stabilire un’alterata nocicezione (24). Sul termine “nociplastico” il dibattito è ancora acceso e qualche autore ha proposto di cambiare il termine in “dolore centralizzato” (25). Questa definizione tuttavia non può essere considerata corretta in quanto implica una descrizione anatomica a fronte delle altre due definizioni (nocicettivo e neuropatico) che descrivono il dolore dal punto di vista fisiologico. Inoltre, implica che tutte le forme di dolore nociplastico siano di origine centrale, ma questo deve essere ancora dimostrato (26).
Il termine “dolore nociplastico” quindi è utile in clinica, ma non può essere usato come diagnosi o come sinonimo di sensibilizzazione centrale (27).
Conclusione
La sensibilizzazione centrale è un meccanismo di elaborazione del dolore in cui si ha un aumento delle reattività dei neuroni spinali, accompagnato da una diminuzione della modulazione discendente inibitoria. Clinicamente è responsabile di fenomeni quali iperalgesia secondaria, allodinia e allargamento del campo recettoriale. Al contrario della sensibilizzazione periferica, essa non dipende da un’alterazione della nocicezione quanto piuttosto da un cambiamento delle proprietà dei neuroni del SNC. Il protrarsi della sensibilizzazione dei neuroni di II ordine oltre la guarigione tissutale è causa di cambiamenti strutturali e funzionali a livello della matrice corticale, responsabili dello sviluppo e del mantenimento del dolore cronico (28)(29).
-
- IASP Terminology “Part III: Pain Terms, A Current List with Definitions and Notes on Usage” (pp 209-214) Classification of Chronic Pain, Second Edition, IASP Task Force on Taxonomy, edited by H. Merskey and N. Bogduk, IASP Press, Seattle, 1994
- Woolf CJ. Central sensitization: implications for the diagnosis and treatment of pain. 2011;152(3 Suppl):S2-15.
- Nijs J, Torres-cueco R, Van wilgen CP, et al. Applying modern pain neuroscience in clinical practice: criteria for the classification of central sensitization pain. Pain Physician. 2014;17(5):447-57.
- Smart KM, Blake C, Staines A, Doody C. The Discriminative validity of “nociceptive,” “peripheral neuropathic,” and “central sensitization” as mechanisms-based classifications of musculoskeletal pain. Clin J Pain. 2011;27(8):655-63.
- Nijs J, Goubert D, Ickmans K. Recognition and Treatment of Central Sensitization in Chronic Pain Patients: Not Limited to Specialized Care. J Orthop Sports Phys Ther. 2016;46(12):1024-1028.
- Chiarotto A, Viti C, Sulli A, Cutolo M, Testa M, Piscitelli D. Cross-cultural adaptation and validity of the Italian version of the Central Sensitization Inventory. Musculoskelet Sci Pract. 2018;37:20-28.
- Woolf CJ. What is this thing called pain?. J Clin Invest. 2010;120(11):3742-4.
- Williams DA. Phenotypic Features of Central Sensitization. J Appl Biobehav Res. 2018;23(2)
- Williams FM, Spector TD, Macgregor AJ. Pain reporting at different body sites is explained by a single underlying genetic factor. Rheumatology (Oxford). 2010;49(9):1753-5
- Hartvigsen J, Nielsen J, Kyvik KO, et al. Heritability of spinal pain and consequences of spinal pain: a comprehensive genetic epidemiologic analysis using a population-based sample of 15,328 twins ages 20-71 years. Arthritis Rheum. 2009;61(10):1343-51.
- Latremoliere A, Woolf CJ. Central sensitization: a generator of pain hypersensitivity by central neural plasticity. J Pain. 2009;10(9):895-926.
- Mendell LM, Wall PD. RESPONSES OF SINGLE DORSAL CORD CELLS TO PERIPHERAL CUTANEOUS UNMYELINATED FIBRES. 1965;206:97-9.
- Ji RR, Kohno T, Moore KA, Woolf CJ. Central sensitization and LTP: do pain and memory share similar mechanisms?. Trends Neurosci. 2003;26(12):696-705.
- Ji RR, Berta T, Nedergaard M. Glia and pain: is chronic pain a gliopathy?. 2013;154 Suppl 1:S10-28.
- Woolf CJ, Salter MW. Neuronal plasticity: increasing the gain in pain. Science. 2000;288(5472):1765-9.
- Woolf CJ, King AE. Dynamic alterations in the cutaneous mechanoreceptive fields of dorsal horn neurons in the rat spinal cord. J Neurosci. 1990;10(8):2717-26.
- Kregel J, Meeus M, Malfliet A, et al. Structural and functional brain abnormalities in chronic low back pain: A systematic review. Semin Arthritis Rheum. 2015;45(2):229-37
- Adams LM, Turk DC. Psychosocial factors and central sensitivity syndromes. Curr Rheumatol Rev. 2015;11(2):96-108.
- Mizumura K. Peripheral mechanism of hyperalgesia–sensitization of nociceptors. Nagoya J Med Sci. 1997;60(3-4):69-87.
- Graven-nielsen T, Arendt-nielsen L. Peripheral and central sensitization in musculoskeletal pain disorders: an experimental approach. Curr Rheumatol Rep. 2002;4(4):313-21.
- https://www.iasp-pain.org/terminology?navItemNumber=576%23Pain#Nociplasticpain
- Aydede M, Shriver A. Recently introduced definition of “nociplastic pain” by the International Association for the Study of Pain needs better formulation. Pain. 2018;159(6):1176-1177.
- Kosek E, Cohen M, Baron R, Mico JA, Rice AS. Reply. Pain. 2017;158(1):180.
- Kosek E, Cohen M, Baron R, Mico JA, Rice ASC. Reply. Pain. 2018;159(6):1177-1178.
- Brummett C, Clauw D, Harris R, Harte S, Hassett A, Williams D. We agree with the need for a new term but disagree with the proposed terms. Pain. 2016;157(12):2876.
- Trouvin A-P, Perrot s, New Concepts of Pain. Best Pract Res Clin Rheumatol 2019 Jun;33(3):101415. doi: 10.1016/j.berh.2019.04.007. Epub 2019
- Kosek E, Cohen M, Baron R, et al. Do we need a third mechanistic descriptor for chronic pain states?. 2016;157(7):1382-6.
- Apkarian AV, Baliki MN, Geha PY. Towards a theory of chronic pain. Prog Neurobiol. 2009;87(2):81-97.
- Tracey I, Bushnell MC. How neuroimaging studies have challenged us to rethink: is chronic pain a disease?. J Pain. 2009;10(11):1113-20.