Claudicatio vascolare
Ecco una guida per il fisioterapista su valutazione e trattamento della claudicatio vascolare.

La claudicatio intermittens, o claudicatio vascolare, rappresenta il sintomo cardine della malattia arteriosa periferica (PAD), condizione in cui c’è un’ostruzione totale o parziale dei vasi che forniscono sangue dal cuore alla periferia, con riduzione dell’afflusso di sangue agli arti inferiori. Il risultato è un dolore muscolare evocato dallo sforzo, tipicamente alla marcia, che scompare con il riposo1,2.
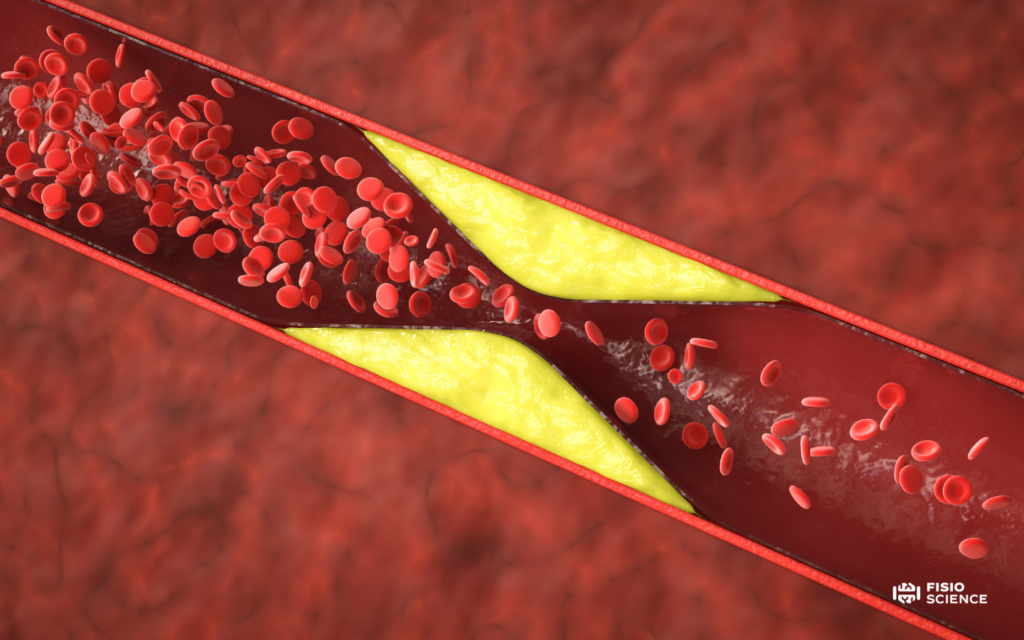
Nonostante la sua apparente semplicità clinica, la claudicatio rappresenta una manifestazione visibile di una malattia sistemica piuttosto complessa, spesso associata ad aterosclerosi generalizzata (un indurimento di un’arteria dovuto alla formazione di una placca ateromasica3), e quindi a un aumentato rischio di eventi cardiovascolari maggiori come infarto e ictus4.
La PAD colpisce principalmente gli arti inferiori e interessa circa il 7% delle persone tra i 55 e i 59 anni, con un incremento progressivo legato all’età che arriva a coinvolgere quasi il 25% degli individui tra i 95 e i 99 anni5. È, inoltre, un alto predittore di mortalità: è stato riportato che la PAD causa un aumento del 60% del rischio di mortalità per tutte le cause, del 96% dei decessi cardiovascolari, del 45% del rischio di sviluppare coronaropatie e del 35% del rischio di sviluppare una malattia cerebrovascolare6.
Un aspetto importante da notare che dal 20 al 50% dei soggetti con PAD non presenta sintomi clinici evidenti; tuttavia, quando la perfusione non è più sufficiente a soddisfare le richieste metaboliche dei tessuti, compaiono i sintomi tipici della malattia7.
La PAD è stata classificata da Fontaine e da Rutherford in diversi stadi e gradi.
| Fontaine’s staging of PAD | Rutherford’s grading of PAD | |||
|---|---|---|---|---|
| Stage | Clinical finding | Grade | Category | Clinical finding |
| I | Asymptomatic | 0 | 0 | Asymptomatic |
| IIa | Mild claudication, symptoms at distances >200 m | I | 1 | Mild claudication |
| IIb | Moderate-to-severe claudication, symptoms at <200 m | I | 2 | Moderate claudication |
| IIb | Severe claudication | I | 3 | Severe claudication |
| III | Ischemic rest pain | II | 4 | Ischemic rest pain |
| IV | Ulceration and/or gangrene | III | 5 | Minor tissue loss |
| IV | Ulceration and/or gangrene | III | 6 | Major tissue loss |
Dal punto di vista del fisioterapista e del medico, riconoscere la claudicatio precocemente è cruciale: permette di impostare un percorso diagnostico efficace e un programma riabilitativo basato su esercizio mirato e prevenire complicanze invalidanti.
Tipologia di paziente
Il paziente con disturbo arterioso periferico è in genere un adulto o anziano con fattori di rischio cardiovascolare noti: storia personale o familiare di patologie cardiovascolari8, soggetto fumatore9 o sedentario, storia di diabete mellito10, ipertensione, dislipidemia, insufficienza renale7 e uso di farmaci beta-bloccanti7.
Il dolore è tipicamente localizzato al polpaccio, ma può interessare anche la coscia o i glutei in base al livello dell’occlusione arteriosa (aorto-iliaca, femorale o poplitea). Si tratta di un dolore acuto, spesso descritto come pulsante o crampiforme. Possono presentarsi anche parestesie e intorpidimento, sensazione di fatica muscolare, alterazioni cutanee (come pallore, cianosi, rossore) e del letto ungueale, cambiamenti della temperatura corporea, possibile presenza di edema, lesioni trofiche, tempo di riempimento capillare >3 secondi e polsi periferici ridotti o assenti.
Per questo motivo è fondamentale confrontare sempre i due lati ed effettuare un esame accurato dell’apparato tegumentario e neurovascolare periferico1. È importante ricordare che molti pazienti con PAD sono asintomatici o presentano sintomi atipici come dolore diffuso, crampi notturni e debolezza, i quali ritardano la diagnosi11.
In molti casi, il soggetto riferisce una progressiva riduzione della distanza di marcia nel tempo: inizialmente può camminare centinaia di metri prima dell’insorgenza del dolore, ma con l’avanzare della malattia il fastidio compare dopo pochi passi12.
Patofisiologia
La claudicatio intermittens rappresenta la manifestazione funzionale dell’insufficienza arteriosa cronica degli arti inferiori. Il meccanismo primario è l’aterosclerosi13,14, che causa stenosi e una progressiva riduzione del flusso ematico distale.
Durante l’attività muscolare, la richiesta di ossigeno aumenta, ma l’apporto non riesce a soddisfarla, determinando così un’ischemia relativa. Il risultato è un accumulo di metaboliti vasodilatatori e acidi, come lattato e adenosina, che stimolano i nocicettori muscolari e generano il dolore2,15. Si tratta di una risposta adattativa, quasi “di sopravvivenza”, in cui i tessuti ischemici riducono il proprio consumo di ossigeno per far fronte alla scarsa disponibilità.
Con il tempo, il muscolo ischemico subisce alterazioni strutturali e metaboliche: riduzione delle fibre ossidative, disfunzione mitocondriale e aumentata produzione di specie reattive dell’ossigeno15. Questi cambiamenti spiegano perché, anche dopo una rivascolarizzazione tecnicamente efficace, molti pazienti continuano a presentare ridotta performance muscolare.
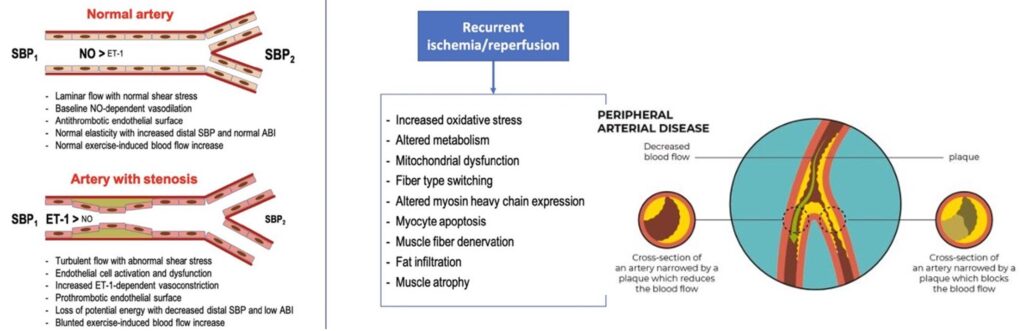
La distinzione tra una PAD asintomatica16 e la claudicatio intermittens dipende principalmente da tre fattori: il livello di attività fisica del soggetto, l’estensione del processo aterosclerotico e la capacità del sistema vascolare di creare circoli collaterali.
Come suggerisce il termine latino claudicare (“zoppicare”), i sintomi si manifestano solo durante lo sforzo e regrediscono con il riposo entro 5-10 minuti17, rendendo la condizione “intermittente” per definizione. Paradossalmente, l’attività fisica che scatena il dolore rappresenta anche lo strumento più efficace per contrastare la progressione della malattia18.
Diagnosi differenziale
La claudicatio vascolare va distinta da altre condizioni che possono causare dolore da sforzo agli arti inferiori, in particolare dalla claudicatio neurogena dovuta a stenosi lombare e dalle mialgie da cause ortopediche o metaboliche14,19.
| Neurogenica | Vascolare | |
|---|---|---|
| Dolore alla gamba | Prossimale → Distale | Distale → Prossimale |
| Sollievo | Da seduto, sdraiato | In piedi |
| Dolore da supino | Negativo | Sollievo nel mettersi in piedi |
| Camminare | Meglio in salita | Meglio in discesa |
| Bici | Negativo | Causa dolore |
| Flessione lombare | Sollievo | Nessun effetto |
| Estensione lombare | Peggiora | Nessun effetto |
| Polso periferico | Normale | Debole |
| Cute | Normale | Perdita di peli, disturbi trofici |
| Postura | In flessione | Normale |
Altre patologie associate a sintomi alle gambe, come stenosi spinale, radicolopatie lombosacrali, neuropatie periferiche, artrosi, insufficienza venosa cronica e traumi ossei o legamentosi possono mimare o anche sovrapporsi alla malattia arteriosa periferica18,20,21. Una diagnosi differenziale accurata è fondamentale per evitare trattamenti inappropriati e indirizzare correttamente il paziente allo specialista vascolare quando necessario.
Nella pratica clinica, il fisioterapista può incontrare sia pazienti con PAD nota sia con PAD non ancora diagnosticata. Con l’evoluzione della professione verso una maggiore autonomia, diventa essenziale saper riconoscere precocemente i segni di una PAD non identificata, garantendo la sicurezza del paziente e l’invio tempestivo al medico.
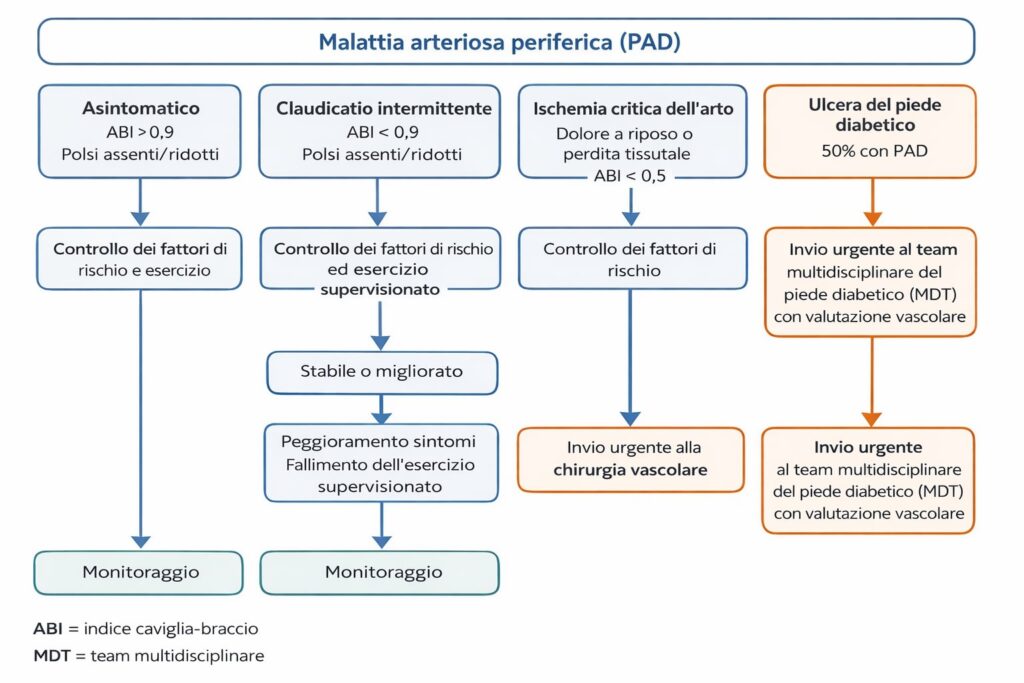
Alcuni segnali d’allarme che richiedono un invio urgente allo specialista vascolare sono: comparsa acuta delle “6P”, dolore a riposo al piede da oltre due settimane, ulcere che non guariscono, presenza di cancrena. I pazienti con polsi periferici ridotti, dolore atipico o claudicatio non ancora indagata, dovrebbero invece essere indirizzati al medico di base o ai servizi territoriali.
Il fisioterapista ha inoltre un ruolo chiave nel monitorare l’evoluzione clinica del paziente e favorire una diagnosi tempestiva in caso di peggioramento clinico, oltre ad essere la figura responsabile della prescrizione e gestione dell’esercizio terapeutico nei pazienti con PAD.
Elementi anamnestici
In anamnesi bisogna indagare i fattori sottostanti.
- Fattori di rischio: fumo, diabete, dislipidemia, ipertensione, patologie cardiovascolari concomitanti.
- Caratteristiche del dolore: sede, intensità, modalità d’insorgenza e regressione.
- Distanza di marcia: quanti metri riesce a percorrere prima del dolore (importante anche per monitorare i miglioramenti).
- Eventuali sintomi associati: freddo agli arti, pallore, formicolii, ulcere trofiche.
Un elemento chiave è la reversibilità del dolore con il riposo: il dolore ischemico muscolare tipicamente scompare entro 5-10 minuti dall’interruzione dello sforzo4.
Esame obiettivo e valutazione
L’esame obiettivo si concentra sulla valutazione vascolare periferica. I principali step sono descritti di seguito.
- Ispezione: bisogna ricercare la presenza di cute secca, pallore, ridotta crescita di peli nell’area ischemica, atrofia muscolare della muscolatura coinvolta, eventuali ulcere trofiche.
- Palpazione dei polsi periferici: possono risultare ridotti o assenti. Tra tutti i reperti clinici, questo è l’elemento più importante nella prima inquadratura del paziente. Quando i polsi femorali non sono palpabili, è più probabile che il problema riguardi il tratto aorto-iliaco, cioè la zona di afflusso del sangue. Al contrario, se il polso femorale è presente ma risultano deboli o assenti il popliteo o i polsi distali (tibiale posteriore e pedidio), il sospetto si sposta verso una malattia dell’efflusso, in particolare femoro-poplitea e/o tibiale22,24.
- Misurazione della pressione sanguigna e della frequenza cardiaca per monitorare il profilo cardiovascolare.
- Auscultazione di soffi vascolari con fonendoscopio.
- Test di Buerger: può essere eseguito o attraverso l’elevazione dell’arto a 45° fino a comparsa di pallore, seguita da iperemia reattiva; oppure mantenendo gli arti inferiori in elevazione per 2 minuti, facendoli poi penzolare oltre il bordo del letto per osservare la presenza di iperemia reattiva25.
Dal punto di vista strumentale, la misurazione dell’ABI (Ankle-Brachial Index) rappresenta lo standard diagnostico non invasivo: viene calcolato per ciascuna gamba dividendo la pressione sistolica più elevata dell’arteria tibiale posteriore o dorsale del piede per la pressione sistolica più elevata dell’arteria brachiale destra o sinistra. Un valore < 0,9 è indicativo di PAD18,26.
Nei centri specializzati si può ricorrere a eco-Doppler, angio-TC o angio-RM per localizzare con precisione il livello della stenosi.
Nel contesto fisioterapico, la valutazione funzionale tramite test del cammino su treadmill è utile per quantificare la distanza percorsa fino all’insorgenza del dolore e per valutare i progressi dopo l’intervento riabilitativo2.
Trattamento
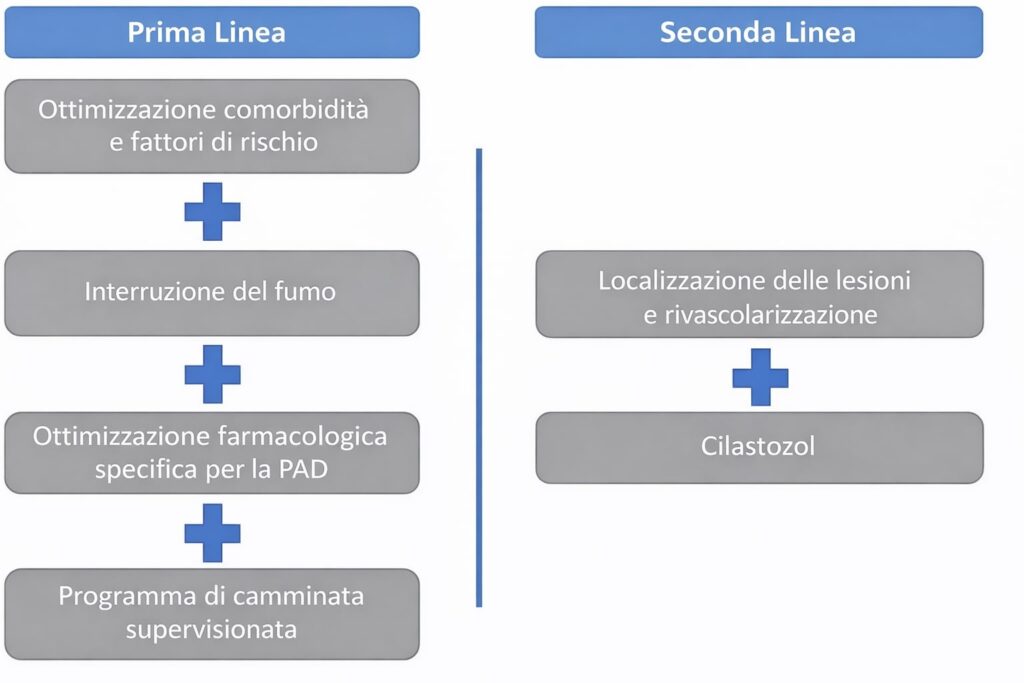
La gestione iniziale della claudicatio intermittens prevede innanzitutto una ottimizzazione della terapia medica e il controllo dei principali fattori di rischio, come ipertensione, diabete e dislipidemia, insieme alla cessazione del fumo7,23,24,28. A questi interventi generali si affianca la gestione specifica per la PAD, che comprende l’assunzione quotidiana di aspirina e la terapia con statine, che riducono rispettivamente gli eventi cardiovascolari e la progressione dell’aterosclerosi. L’altro elemento centrale della prima linea di trattamento è l’avvio di un programma di terapia fisica supervisionata (SET)29.
Come passo successivo, nei pazienti che lo possono assumere, si considera l’introduzione del cilostazolo e del naftidrofurile30,31. Infine, nei casi in cui la terapia medica sia stata ottimizzata e il programma di esercizio supervisionato completato senza miglioramento significativo dei sintomi, si può prendere in considerazione una procedura di rivascolarizzazione.
Terapia fisica supervisionata (SET)
La SET prevede sessioni di 30-45 minuti, almeno 3 volte a settimana per minimo 12 settimane, con camminate fino a dolore moderato seguite da pause di recupero22,32; anche se per quanto riguarda il dosaggio degli esercizi ci sono differenze tra le linee guida perché molti pazienti, soprattutto nelle prime settimane, potrebbero non raggiungere questi obiettivi e il percorso riabilitativo deve essere impostato con un criterio di progressione graduale.
Studi clinici mostrano che ci sono miglioramenti significativi nella distanza percorsa, nella qualità di vita, nella salute mentale e nella funzione endoteliale31, ma non risultano variazioni significative dell’ABI.

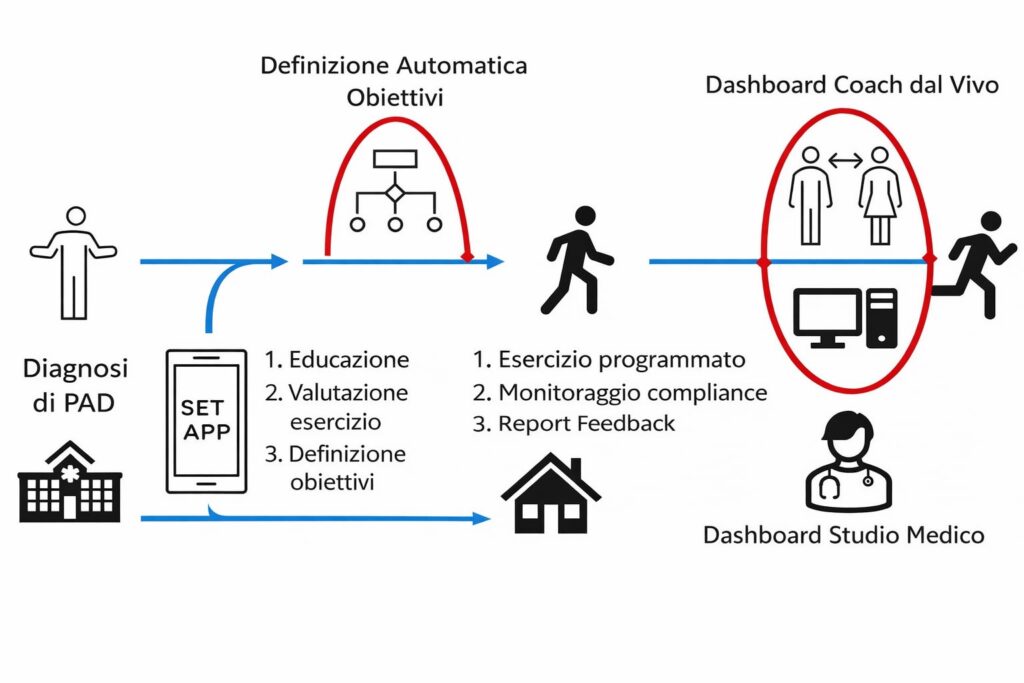
Per favorire una diffusione più ampia della SET, la Society of Vascular Surgery ha sviluppato una applicazione per smartphone che facilita l’interazione tra pazienti, medici, fisioterapisti, allenatori e tutto il team multidisciplinare coinvolto. L’obiettivo è migliorare l’aderenza e la qualità del programma domiciliare. L’impatto reale di questo strumento, così come i risultati a lungo termine, deve però ancora essere confermato da studi dedicati.
I programmi di SET per persone con PAD devono essere adattati alle caratteristiche individuali, considerando durata, intensità, frequenza e rapporto lavoro-riposo. La letteratura disponibile fornisce comunque indicazioni utili per definire questi parametri.
| Modalità | Camminata sul tapis roulant supervisionata |
| Intensità | Carico di lavoro massimo del 40%-60% basato sul test di base sul tapis roulant o carico di lavoro che provoca claudicazione entro 3-5 minuti durante un 6-MWT |
| Durata della sessione | 30-50 minuti di esercizio intermittente; l’obiettivo è accumulare almeno 30 minuti di esercizio di camminata |
| Intensità della claudicazione | Claudicazione da moderata a moderata/grave, se tollerata |
| Rapporto lavoro-riposo | La durata della camminata dovrebbe essere compresa tra 5 e 10 minuti per raggiungere una claudicazione da moderata a moderatamente grave, seguita da riposo fino alla scomparsa del dolore (2-5 minuti) |
| Frequenza | 3 volte a settimana supervisionato |
| Durata del programma | Almeno 12 settimane |
| Progressione | Ogni 1-2 settimane: aumentare la durata della sessione di allenamento per raggiungere i 50 minuti. Poiché gli individui possono camminare oltre i 10 minuti senza raggiungere il livello di claudicazione prescritto, modificare il grado o la velocità della prescrizione dell’esercizio per mantenere le sessioni di camminata entro i 5-10 minuti. |
| Manutenzione | Manutenzione a vita almeno 2 volte a settimana |
L’obiettivo è portare gradualmente il paziente a raggiungere 30-45 minuti complessivi di camminata su tapis roulant per ogni sessione. L’intensità consigliata è quella che induce un lieve dolore da claudicatio entro circa 5 minuti, e un dolore da moderato a moderatamente intenso entro 10 minuti, dopodiché si effettua una pausa finché il fastidio non scompare del tutto. I principali RCT che hanno riportato miglioramenti significativi nella capacità di cammino utilizzavano un protocollo di 3 sessioni settimanali32.
Per quanto riguarda la scelta dell’attività, la camminata rimane l’opzione più efficace per migliorare la capacità di deambulazione, mentre modalità alternative come il ciclismo o l’esercizio aerobico per gli arti superiori sembrano favorire maggiormente il miglioramento della fitness cardiorespiratoria.
Per quanto riguarda l’intensità, l’esercizio a bassa intensità può offrire benefici simili a quello ad alta intensità, purché la durata complessiva dell’allenamento venga aumentata per garantire un’esposizione equivalente allo stimolo.
È stato osservato anche che utilizzare come obiettivo l’avvicinarsi al dolore quasi massimale, piuttosto che fermarsi ai primi segni di fastidio, determina miglioramenti più evidenti sia nella distanza alla comparsa del dolore sia nella distanza massimale.
Tuttavia, va ricordato che questi dati derivano principalmente da protocolli su tapis roulant basati sul tempo al dolore massimale, che potrebbero sottostimare i vantaggi reali nelle attività quotidiane, generalmente svolte a intensità submassimale34,35.
Di conseguenza, è opportuno orientare il programma verso un piano personalizzato, costruito sulle esigenze e sugli obiettivi specifici del paziente36.
Quando la terapia SET non è disponibile, si può prendere in considerazione una terapia fisica alternativa non supervisionata. Ai pazienti possono essere prescritti programmi di camminata chiari, facilmente seguibili a casa e progettati per ottenere gli stessi risultati funzionali della terapia SET tradizionale37.
I test funzionali e questionari specifici e generali più utilizzati per la valutazione di pazienti con PAD sono descritti nella tabella sottostante.
| Utilità | Misura primaria | Rileva l’effetto del trattamento | Prevede i risultati nella PAD | |
| Test da sforzo | ||||
| Tapis roulant graduato | Misura oggettiva delle massime prestazioni di esercizio | Tempo massimo di camminata sul tapis roulant | Allenamento fisico Farmacoterapia Rivascolarizzazione Compressione pneumatica intermittente |
Mortalità (38) |
| 6-MWT | Misura oggettiva della distanza massima percorribile a piedi, misurata in un corridoio | Distanza massima percorsa in 6 minuti |
Supplemento per l’allenamento fisico (39) Compressione pneumatica intermittente (40) |
Perdita di mobilità Mortalità per tutte le cause Mortalità cardiovascolare Eventi cardiovascolari (41–43) |
| Plantar flexion test | capacità di tollerare l’esercizio in condizioni di ridotta perfusione | numero di sollevamenti sulle punte eseguiti fino all’insorgenza del dolore da claudicatio o all’affaticamento | Allenamento fisico è sensibile ai cambiamenti dopo interventi terapeutici | tolleranza allo sforzo velocità di progressione delle limitazioni della PAD. |
| Monitor dell’attività fisica | ||||
| Accelerometro | Misura oggettiva dell’attività durante la vita quotidiana | Dispositivo indossabile | Allenamento fisico | Mortalità Perdita di mobilità (44,45) |
| Questionari generali | ||||
| MOS SF-36 | Qualità della vita correlata alla salute (HRQOL) | Funzione fisica e mentale | Allenamento fisico Farmacoterapia Rivascolarizzazione |
|
| EQ-5D | Stato funzionale e qualità della vita correlata alla salute | Stato di salute e funzionalità | Allenamento fisico Rivascolarizzazione |
|
| Questionari specifici per PAD | ||||
| WIQ | Stato funzionale | Distanza, velocità, scale e gravità della claudicazione | Allenamento fisico Farmacoterapia Rivascolarizzazione |
Prevede la mortalità per tutte le cause e cardiovascolare (46) |
| VascuQoL | Stato funzionale, HRQOL | Dolore, sintomi, attività, emotivo, sociale | Allenamento fisico Rivascolarizzazione |
|
| PAQ | Stato funzionale e soddisfazione della salute | Funzione fisica, soddisfazione per la cura | Allenamento fisico Rivascolarizzazione Terapia medica |
|
| PADQOL | Qualità della vita correlata alla salute (HRQOL) | Sintomi/limitazioni fisiche, paura/incertezza, interazioni sociali, senso di sé, stati emotivi, adattamento | Allenamento fisico | |
In caso di fallimento della terapia conservativa o di ischemia critica, si ricorre a angioplastica o bypass chirurgico, preferibilmente dopo valutazione multidisciplinare. Le attuali linee guida professionali suggeriscono che i pazienti con claudicatio intermittens siano trattati con un approccio conservativo (ovvero con terapie di prima e seconda linea come descritto sopra) per un minimo di 3-6 mesi prima di prendere in considerazione la rivascolarizzazione.
Prognosi
La prognosi della claudicatio intermittens dipende principalmente dal controllo dei fattori di rischio sistemici più che dall’evoluzione locale. Solo una minoranza dei pazienti (15-20%) progredisce verso ischemia critica o amputazione, ma il rischio di eventi cardiovascolari è 3-6 volte superiore rispetto alla popolazione generale2,47.
Per questo motivo, la gestione deve essere multidisciplinare, coinvolgendo medico di base, angiologo, fisioterapista e, quando opportuno, lo specialista in riabilitazione vascolare. Un percorso di riabilitazione vascolare strutturata, associata ad un’adeguata educazione sanitaria e al monitoraggio periodico dell’ABI rappresenta la strategia più efficace per migliorare sia la prognosi sia la qualità di vita del paziente29.
-
-
-
Feller D, Giudice A, Faletra A, Salomon M, Galeno E, Rossettini G, et al.
[Internet]. 2022 Oct 1 [cited 2025 Nov 10];61:102611. Available from: https://www.sciencedirect.com/science/article/pii/S2468781222001114?via%3Dihub- Hiatt WR. Medical treatment of peripheral arterial disease and claudication. N Engl J Med [Internet]. 2001 May 24 [cited 2025 Nov 10];344(21):1608–21. Available from: https://pubmed.ncbi.nlm.nih.gov/11372014/
- Firnhaber JM, Powell CS. Lower Extremity Peripheral Artery Disease: Diagnosis and Treatment. Am Fam Physician [Internet]. 2019 Mar 15 [cited 2025 Nov 10];99(6):362–9. Available from: https://www.aafp.org/pubs/afp/issues/2019/0315/p362.html
- Criqui MH, Aboyans V. Epidemiology of peripheral artery disease. Circ Res [Internet]. 2015 Apr 24 [cited 2025 Nov 10];116(9):1509–26. Available from: https://pubmed.ncbi.nlm.nih.gov/25908725/
- Fowkes FGR, Rudan D, Rudan I, Aboyans V, Denenberg JO, McDermott MM, et al. Comparison of global estimates of prevalence and risk factors for peripheral artery disease in 2000 and 2010: A systematic review and analysis. The Lancet [Internet]. 2013 [cited 2025 Nov 10];382(9901):1329–40. Available from: https://pubmed.ncbi.nlm.nih.gov/23915883/
- Heald CL, Fowkes FGR, Murray GD, Price JF. Risk of mortality and cardiovascular disease associated with the ankle-brachial index: Systematic review. Atherosclerosis [Internet]. 2006 Nov [cited 2025 Nov 15];189(1):61–9. Available from: https://pubmed.ncbi.nlm.nih.gov/16620828/
- Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FGR. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). J Vasc Surg [Internet]. 2007 Jan [cited 2025 Nov 10];45(1 SUPPL.). Available from: https://pubmed.ncbi.nlm.nih.gov/17223489/
- Joosten MM, Pai JK, Bertoia ML, Rimm EB, Spiegelman D, Mittleman MA, et al. Associations Between Conventional Cardiovascular Risk Factors and Risk of Peripheral Artery Disease in Men. JAMA [Internet]. 2012 Oct 24 [cited 2025 Nov 14];308(16):1660–7. Available from: https://jamanetwork.com/journals/jama/fullarticle/1386609
- Willigendael EM, Teijink JAW, Bartelink ML, Kuiken BW, Boiten J, Moll FL, et al. Influence of smoking on incidence and prevalence of peripheral arterial disease. J Vasc Surg [Internet]. 2004 Dec 1 [cited 2025 Nov 14];40(6):1158–65. Available from: https://www.sciencedirect.com/science/article/pii/S0741521404011413
- Selvin E, Marinopoulos S, Berkenblit G, Rami T, Brancati FL, Powe NR, et al. Meta-Analysis: Glycosylated Hemoglobin and Cardiovascular Disease in Diabetes Mellitus. https://doi.org/107326/0003-4819-141-6-200409210-00007 [Internet]. 2004 Sep 21 [cited 2025 Nov 14];141(6). Available from: /doi/pdf/10.7326/0003-4819-141-6-200409210-00007?download=true
- Aboyans V, Ricco JB, Bartelink MLEL, Björck M, Brodmann M, Cohnert T, et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal…. Eur Heart J [Internet]. 2018 Mar 1 [cited 2025 Nov 10];39(9):763–816. Available from: https://pubmed.ncbi.nlm.nih.gov/28886620/
- McDermott MMG, Greenland P, Liu K, Guralnik JM, Criqui MH, Dolan NC, et al. Leg symptoms in peripheral arterial disease: associated clinical characteristics and functional impairment. JAMA [Internet]. 2001 Oct 3 [cited 2025 Nov 14];286(13):1599–606. Available from: https://pubmed.ncbi.nlm.nih.gov/11585483/
- Ankle brachial index for the diagnosis of lower limb peripheral arterial disease – Crawford, F – 2016 | Cochrane Library [Internet]. [cited 2025 Nov 14]. Available from: https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD010680.pub2/full
- Hirsch AT, Haskal ZJ, Hertzer NR, Bakal CW, Creager MA, Halperin JL, et al. ACC/AHA 2005 Practice Guidelines for the management of patients with peripheral arterial disease (lower extremity, renal, mesenteric, and abdominal aortic): a collaborative report from the American Association for Vascular Surgery/Society for Vascular Su…. Circulation [Internet]. 2006 [cited 2025 Nov 15];113(11):e463–654. Available from: https://pubmed.ncbi.nlm.nih.gov/16549646/
- Pipinos II, Judge AR, Selsby JT, Zhu Z, Swanson SA, Nella AA, et al. The myopathy of peripheral arterial occlusive disease: Part 2. Oxidative stress, neuropathy, and shift in muscle fiber type. Vasc Endovascular Surg [Internet]. 2008 Apr [cited 2025 Nov 14];42(2):101–12. Available from: https://pubmed.ncbi.nlm.nih.gov/18390972/
- Alahdab F, Wang AT, Elraiyah TA, Malgor RD, Rizvi AZ, Lane MA, et al. A systematic review for the screening for peripheral arterial disease in asymptomatic patients. J Vasc Surg [Internet]. 2015 Mar 1 [cited 2025 Nov 14];61(3):42S-53S. Available from: https://www.sciencedirect.com/science/article/pii/S0741521414022836
- Hamburg NM, Creager MA. Fisiopatologia della claudicatio intermittens nella malattia arteriosa periferica. Circulation Journal [Internet]. 2017 [cited 2025 Nov 14];81(3):281–9. Available from: https://www.scopus.com/pages/publications/85013923210?inward
- Stonko DP, Hicks CW. Current Management of Intermittent Claudication. Adv Surg [Internet]. 2023 Sep 1 [cited 2025 Nov 14];57(1):103. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC10773527/
- Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FGR. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). J Vasc Surg [Internet]. 2007 Jan 1 [cited 2025 Nov 14];45(1):S5–67. Available from: https://www.sciencedirect.com/science/article/pii/S0741521406022968
- Campia U, Gerhard-Herman M, Piazza G, Goldhaber SZ. Peripheral Artery Disease: Past, Present, and Future. American Journal of Medicine [Internet]. 2019 Oct 1 [cited 2025 Nov 15];132(10):1133–41. Available from: https://pubmed.ncbi.nlm.nih.gov/31150643/
- Feller D, Giudice A, Maritati G, Maselli F, Rossettini G, Meroni R, et al. Physiotherapy Screening for Referral of a Patient with Peripheral Arterial Disease Masquerading as Sciatica: A Case Report. Healthcare [Internet]. 2023 Jun 1 [cited 2025 Nov 15];11(11):1527. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC10252713/
- Gerhard-Herman MD, Gornik HL, Barrett C, Barshes NR, Corriere MA, Drachman DE, et al. 2016 AHA/ACC guideline on the management of patients with lower extremity peripheral artery disease: Executive Summary: A report of the American college of cardiology/American Heart Association task force on clinical practice guidelines. Circulation [Internet]. 2017 [cited 2025 Nov 15];135(12):e686–725. Available from: /doi/pdf/10.1161/CIR.0000000000000470?download=true
- Woo K, Siracuse JJ, Klingbeil K, Kraiss LW, Osborne NH, Singh N, et al. Society for Vascular Surgery appropriate use criteria for management of intermittent claudication. J Vasc Surg [Internet]. 2022 Jul 1 [cited 2025 Nov 15];76(1):3-22.e1. Available from: https://pubmed.ncbi.nlm.nih.gov/35470016/
- Conte MS, Pomposelli FB, Clair DG, Geraghty PJ, McKinsey JF, Mills JL, et al. Society for Vascular Surgery practice guidelines for atherosclerotic occlusive disease of the lower extremities: Management of asymptomatic disease and claudication. J Vasc Surg [Internet]. 2015 Mar 1 [cited 2025 Nov 15];61(3):2S-41S.e1. Available from: https://pubmed.ncbi.nlm.nih.gov/25638515/
- Bailey MA, Griffin KJ, Scott DJA. Clinical Assessment of Patients with Peripheral Arterial Disease. Semin Intervent Radiol [Internet]. 2014 [cited 2025 Nov 16];31(4):292. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC4232424/
- Aboyans V, Ricco JB, Bartelink MLEL, Björck M, Brodmann M, Cohnert T, et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal…. Eur Heart J [Internet]. 2018 Mar 1 [cited 2025 Nov 16];39(9):763–816. Available from: https://pubmed.ncbi.nlm.nih.gov/28886620/
- Morley RL, Sharma A, Horsch AD, Hinchliffe RJ. Peripheral artery disease. BMJ [Internet]. 2018 [cited 2025 Nov 16];360. Available from: https://pubmed.ncbi.nlm.nih.gov/29419394/
- Gerhard-Herman MD, Gornik HL, Barrett C, Barshes NR, Corriere MA, Drachman DE, et al. 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation [Internet]. 2016 [cited 2025 Nov 15];135(12):e686. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC5479414/
- Treat-Jacobson D, McDermott MM, Bronas UG, Campia U, Collins TC, Criqui MH, et al. Optimal Exercise Programs for Patients with Peripheral Artery Disease: A Scientific Statement from the American Heart Association. Circulation [Internet]. 2019 Jan 22 [cited 2025 Nov 16];139(4):E10–33. Available from: /doi/pdf/10.1161/CIR.0000000000000623?download=true
- Conte MS, Bradbury AW, Kolh P, White J V., Dick F, Fitridge R, et al. Global vascular guidelines on the management of chronic limb-threatening ischemia. Eur J Vasc Endovasc Surg [Internet]. 2019 Jul 1 [cited 2025 Nov 16];58(1 Suppl):S1. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC8369495/
- McDermott MM, Ades P, Guralnik JM, Dyer A, Ferrucci L, Liu K, et al. TREADMILL EXERCISE AND RESISTANCE TRAINING IN PATIENTS WITH PERIPHERAL ARTERIAL DISEASE WITH AND WITHOUT INTERMITTENT CLAUDICATION: A RANDOMIZED CONTROLLED TRIAL. JAMA [Internet]. 2009 Jan 14 [cited 2025 Nov 16];301(2):165. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC3268032/
- Lane R, Harwood A, Watson L, Leng GC. Exercise for intermittent claudication. Cochrane Database Syst Rev [Internet]. 2017 Dec 26 [cited 2025 Nov 16];2017(12):CD000990. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC6486315/
- Treat-Jacobson D, McDermott MM, Bronas UG, Campia U, Collins TC, Criqui MH, et al. Optimal Exercise Programs for Patients with Peripheral Artery Disease: A Scientific Statement from the American Heart Association. Circulation [Internet]. 2019 Jan 22 [cited 2025 Nov 16];139(4):E10–33. Available from: /doi/pdf/10.1161/CIR.0000000000000623?download=true
- Gardner AW, Montgomery PS, Flinn WR, Katzel LI. The effect of exercise intensity on the response to exercise rehabilitation in patients with intermittent claudication. J Vasc Surg [Internet]. 2005 Oct [cited 2025 Nov 16];42(4):702–9. Available from: https://pubmed.ncbi.nlm.nih.gov/16242558/
- Programmi di riabilitazione fisica per il trattamento del dolore da claudicatio. Una meta-analisi – PubMed [Internet]. [cited 2025 Nov 16]. Available from: https://pubmed.ncbi.nlm.nih.gov/7674529/
- Fassora M, Calanca L, Jaques C, Mazzolai L, Kayser B, Lanzi S. Intensity-dependent effects of exercise therapy on walking performance and aerobic fitness in symptomatic patients with lower-extremity peripheral artery disease: A systematic review and meta-analysis. Vascular Medicine (United Kingdom) [Internet]. 2022 Apr 1 [cited 2025 Nov 16];27(2):158–70. Available from: /doi/pdf/10.1177/1358863X211034577?download=true
- Waddell A, Seed S, Broom DR, McGregor G, Birkett ST, Harwood AE. Safety of home-based exercise for people with intermittent claudication: A systematic review. Vascular Medicine (United Kingdom) [Internet]. 2022 Apr 1 [cited 2025 Nov 16];27(2):186–92. Available from: /doi/pdf/10.1177/1358863X211060388?download=true
- Leeper NJ, Myers J, Zhou M, Nead KT, Syed A, Kojima Y, et al. Exercise capacity is the strongest predictor of mortality in patients with peripheral arterial disease. J Vasc Surg [Internet]. 2013 Mar [cited 2025 Nov 16];57(3):728–33. Available from: https://pubmed.ncbi.nlm.nih.gov/23044259/
- McDermott MM, Leeuwenburgh C, Guralnik JM, Tian L, Sufit R, Zhao L, et al. Effect of Resveratrol on Walking Performance in Older People With Peripheral Artery Disease: The RESTORE Randomized Clinical Trial. JAMA Cardiol [Internet]. 2017 Aug 1 [cited 2025 Nov 16];2(8):902. Available from: https://pmc.ncbi.nlm.nih.gov/articles/PMC5815080/
- Chang ST, Hsu J Te, Chu CM, Pan KL, Jang SJ, Lin PC, et al. Using intermittent pneumatic compression therapy to improve quality of life for symptomatic patients with infrapopliteal diffuse peripheral obstructive disease. Circ J [Internet]. 2012 [cited 2025 Nov 16];76(4):971–6. Available from: https://pubmed.ncbi.nlm.nih.gov/22307382/
- McDermott MMG, Liu K, Greenland P, Guralnik JM, Criqui MH, Chan C, et al. Functional decline in peripheral arterial disease: associations with the ankle brachial index and leg symptoms. JAMA [Internet]. 2004 Jul 28 [cited 2025 Nov 16];292(4):453–61. Available from: https://pubmed.ncbi.nlm.nih.gov/15280343/
- McDermott MM, Guralnik JM, Tian L, Ferrucci L, Liu K, Liao Y, et al. Baseline Functional Performance Predicts the Rate of Mobility Loss in Persons With Peripheral Arterial Disease. J Am Coll Cardiol [Internet]. 2007 Sep 4 [cited 2025 Nov 16];50(10):974–82. Available from: https://pubmed.ncbi.nlm.nih.gov/17765125/
- McDermott MM, Greenland P, Tian L, Kibbe MR, Green D, Zhao L, et al. Association of 6-Minute Walk Performance and Physical Activity With Incident Ischemic Heart Disease Events and Stroke in Peripheral Artery Disease. J Am Heart Assoc [Internet]. 2015 Jul 28 [cited 2025 Nov 16];4(7). Available from: https://pubmed.ncbi.nlm.nih.gov/26219563/
- Garg PK, Tian L, Criqui MH, Liu K, Ferrucci L, Guralnik JM, et al. Physical activity during daily life and mortality in patients with peripheral arterial disease. Circulation [Internet]. 2006 Jul [cited 2025 Nov 16];114(3):242–8. Available from: https://pubmed.ncbi.nlm.nih.gov/16818814/
- Garg PK, Liu K, Tian L, Guralnik JM, Ferrucci L, Criqui MH, et al. Physical activity during daily life and functional decline in peripheral arterial disease. Circulation [Internet]. 2009 Jan 20 [cited 2025 Nov 16];119(2):251–60. Available from: https://pubmed.ncbi.nlm.nih.gov/19118256/
- Nead KT, Zhou M, Caceres RD, Olin JW, Cooke JP, Leeper NJ. Walking impairment questionnaire improves mortality risk prediction models in a high-risk cohort independent of peripheral arterial disease status. Circ Cardiovasc Qual Outcomes [Internet]. 2013 May [cited 2025 Nov 16];6(3):255–61. Available from: https://pubmed.ncbi.nlm.nih.gov/23633217/
- Aboyans V, Sevestre MA, Désormais I, Lacroix P, Fowkes G, Criqui MH. Epidemiology of lower extremity artery disease. Presse Medicale [Internet]. 2018 Jan 1 [cited 2025 Nov 16];47(1):38–46. Available from: https://pubmed.ncbi.nlm.nih.gov/29449058/
-
Feller D, Giudice A, Faletra A, Salomon M, Galeno E, Rossettini G, et al.
-
